Otras aplicaciones de la ecografia en la UCIP
- Categoría padre: Cursos de Cardiología Pediátrica
Sumario:
- Introducción
- Ventajas de la ecografía en la UCIP
- Inconvenientes de la ecografía en UCIP
- ¿Qué necesitamos en la UCIP?
- ¿Qué podemos buscar?
- Ecografía torácica:
- Derrame pleural
- Neumotórax
- Derrame pericárdico/ taponamiento cardiaco
- Movilidad diafragmática
- Ecografía abdominal:
- Colecciones intrabdominales
- Valoración del flujo renal
- Valoración de la vejiga
- Sondas gástricas e intestinales
- Ecografía FAST
- Ecografía vascular:
- Canalización de accesos vasculares
- Localización de catéteres
- Trombos intravasculares
- Ecografía cerebral
- Otros usos de la ecografía en UCIP
- Conclusiones
- Bibliografía
En la medicina intensiva es esencial la valoración rápida de los pacientes y la toma de decisiones inmediata en muchos de los casos. Por este motivo es importante tener a nuestro alcance métodos diagnósticos que nos permitan tomar estas decisiones de la forma más eficaz y segura para nuestros pacientes. También es necesario realizar procedimientos en pacientes críticos, generalmente inestables, de una forma eficiente. En este contexto existen múltiples posibilidades, pero es la ecografía la que presenta mayores ventajas en este sentido. La ecografía permite un rápido y detallado examen de los pacientes, sobre todo a pie de cama, con aparatos cada vez más sencillos, más económicos, con mejor calidad y con mayor movilidad.
La realización de una ecografía precisa un material específico, conocimientos anatómicos y un entrenamiento adecuado en la realización de la técnica. Es conocido que en las unidades de cuidados intensivos pediátricos (UCIP) no está disponible un ecografista experto las 24h del día para este tipo de evaluaciones, por este motivo, es importante que los profesionales que trabajan en estas unidades aprendan y se entrenen en la realización de esta técnica tan útil en la practica diaria en la UCIP.
Ventajas de la ecografía:
Se trata de una técnica indolora, incruenta, de realización e interpretación inmediata y que permite la valoración de los órganos en movimiento. No aporta radiación a los pacientes y no tiene efectos secundarios a las longitudes de ondas de trabajo habitual, siendo, por lo tanto, una técnica segura. Aunque se trata de una prueba que depende de la valoración subjetiva del realizador, es fácilmente repetible y versátil. Una de las ventajas fundamentales es que permite la realización de técnicas invasivas apoyadas en la imagen, por lo que se realizarán de forma más segura y rápida, y, en aquellos casos de mayor dificultad, con mayores garantías de éxito. Sin olvidar que las aparatos actuales son móviles, cada vez más sencillos de utilizar y cada vez más económicos.
Inconvenientes de la ecografía:
Aparte de la disponibilidad de un aparato que se ajuste a nuestras necesidades (sencillo, móvil, económico y adaptado a los pacientes pediátricos), es una técnica que precisa una experiencia y un aprendizaje muy importante. Por este motivo, es necesario crear programas de entrenamiento para intensivistas en ecografía. Otro de los potenciales inconvenientes es, al trabajar con pacientes críticos que pueden padecer infecciones nosocomiales, el riesgo de diseminación infecciosa con este procedimiento, si bien es fácilmente salvable con una adecuada protección del aparato y una adecuada limpieza del mismo tras su uso. Al ser una técnica que precisa de la colaboración del paciente (debe estar quieto, tranquilo y en silencio) para obtener una buena calidad de imagen, y en los pacientes pediátricos, en especial, esto puede ser complicado, aunque puede solucionarse con la ayuda de sus padres para tranquilizarlo y, en algunos casos, con la sedación del paciente.
¿Qué necesitamos en la UCIP?
-Ecógrafo y sondas adecuadas. En general precisaremos sondas lineales y curvas de 2,5 a 10MHz para valorar los distintos tipos de estructuras. Si bien es posible adaptar las existentes a nuestras necesidades en función de lo que queramos valorar y el tamaño del paciente. El ecógrafo debe tener al menos las siguientes características: posibilidad de modo M, modo B y Doppler (continuo y pulsado), el Doppler color no es imprescindible aún que si muy útil para algunos técnicas.
-Conocimientos de anatomía: es preciso que el examinador tenga unos conocimientos anatómicos amplios para poder dirigirse a buscar las estructuras de la forma más adecuada, teniendo en cuenta las relaciones anatómicas y las interferencias entre los diferentes órganos y medios físicos.
-Conocimientos ecográficos: De forma básica existen varios conceptos que deben quedar claros. Por una parte, hay que saber que la frecuencia de la sonda nos indica tanto la profundidad óptima del estudio como la calidad de la imagen. De tal forma que sondas de baja frecuencia (2,5-5MHz) nos permiten explorar zonas más profundas pero con peor resolución, por el otro lado, las sondas de alta frecuencia (7,5-10MHz) permiten explorar estructuras superficiales (0,5 a 2mm) pero con alta resolución. El uso de sondas curvas esta indicado cuando la zona a explorar es amplia y profunda, mientras que las lineales son mejores para estudios superficiales y de poco tamaño. Por último, las estructuras líquidas permiten una buena la trasmisión de los ultrasonidos, por lo que en la imagen ecográfica se verán de color negro (anecoico) con ecos bajo las mismas de otras estructuras que permiten ver a su través. Los huesos y el aire, sin embargo, no permiten el paso de los ultrasonidos a su través, por lo que se verán como estructuras blancas (hiperecogénicas), generalmente lineales, sin ecos tras ellas (sombra ecogénica). El resto de estructuras se verán en escala de grises en función de la capacidad para rebotar o dejar pasar los ultrasonidos a su través según su composición química.
-Experiencia: es fundamental que el explorador tenga un entrenamiento en la obtención de las imágenes, incluido el uso del ecógrafo, y en su interpretación para evitar errores en el diagnóstico y en la realización de técnicas.
-Otros: aunque no son imprescindibles, algunos elementos como agujas, sondas, guías sonolucentes, pueden ser muy útiles a la hora de realizar procedimientos guiados por ecografía.
¿Qué podemos buscar?
Las posibilidades de la ecografía en UCIP, tanto para uso diagnóstico como para la realización de técnicas, son muy amplias, por lo que revisaremos en detalle algunas de las más frecuentes y útiles, desde el punto de vista del aparataje, modalidades a utilizar en cada caso y dónde ir a buscar las imágenes más optimas.
-Ecografía torácica:
Es posible la valoración del pulmón, incluidas consolidaciones, atelectasias, etc., pero nos centraremos en lo más útil para los intensivistas: Derrames pleurales (diagnóstico, colocación y localización de catéteres), neumotórax, derrame pericárdico y taponamiento cardiaco (diagnóstico y drenaje), movilidad diafragmática.
-Derrame plural:
Para la localización de derrames pleurales precisaremos un ecógrafo que tenga sondas convexas con frecuencias de 2,5 a 5MHz y utilizaremos dos planos fundamentales, el intercostal inferior (fig. 1) y el subcostal eje corto (fig. 2). Desde estos, en modo B, reorientaremos la sonda hasta que localicemos los espacios pleurales. Hay que tener en cuenta que el derrame pleural es un líquido, en general homogéneo, y por lo tanto anecoico, sobre todo en el caso de los trasudados. Cuando nos encontramos ante un empiema, un exudado o un hemotórax pierde homogeneidad y es más ecogénico, con la posibilidad de visualizar tabiques o tractos fibrosos en forma de elementos hiperecogénicos. Una vez diagnosticado en modo B, se localiza la zona de mayor cuantía, generalmente en la zona mas declive, salvo en colecciones loculadas, realizando en esa zona un corte en modo M donde podemos cuantificar, aproximadamente, en cm el tamaño del derrame.
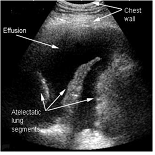 Figura 1
Figura 1 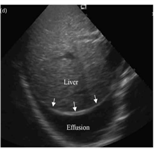 Figura 2
Figura 2
Una vez localizado el derrame podremos señalar la zona de punción para evacuación más óptima, e incluso, guiar la punción con ecografía, de esta forma nos aseguraremos de evitar la interposición de otras estructuras y la punción directa del derrame.
-Neumotórax:
La localización por ecografía de un neumotórax puede ser dificultosa si es de escasa cuantía. Para ello, al encontrarse en localización superficial, utilizaremos sondas de 7,5-10MHz en plano intercostal, intentando identificar una estructura hiperecogénica, lineal y con silencio posterior (fig. 3) al ser aire.
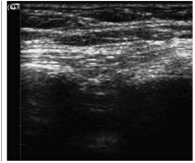 Figura 3
Figura 3
Podemos de la misma forma evacuar el aire guiados por esta imagen ecográfica.
-Derrame pericárdico / taponamiento cardiaco:
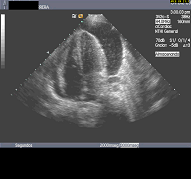
El derrame pericárdico es sencillo de localizar en las proyecciones habituales para le exploración cardiaca, si bien, las mejores para su cuantificación y grado de compromiso son la paraesternal eje largo (fig. 4) y eje corto (video 1) y apical 4 cámaras (fig 6) en modo B, posteriormente paso a modo M (fig. 5) para cuantificar el derrame.
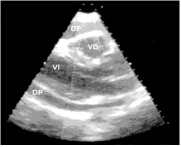 Figura 4
Figura 4 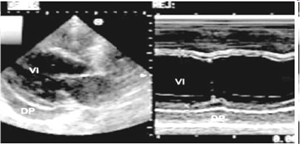 Figura 5
Figura 5
En ocasiones es difícil valorar cuando es preciso drenar este derrame, o lo que es lo mismo, cuando cumple datos de taponamiento y por lo tanto produce repercusión en el paciente. Esto lo identificaremos por la existencia de colapso diastólico de la cavidades cardiacas, en estadios precoces solo las derechas (figs. 6 y 7) (video 1).
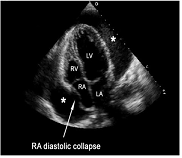 Figura 6
Figura 6 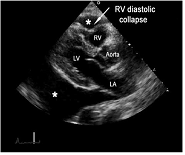 Figura 7
Figura 7
 {jwplayer}&file=eco_ucip_video1.mp4&popup.overidetext=Vídeo 1&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video1.mp4&popup.overidetext=Vídeo 1&jwversion=5_html5{/jwplayer}
Un vez localizado y cuantificado, podemos realizar una punción y colocación de drenaje guiado por ecografía (videos 2 y 3), en general, en aquellos que presenten datos ecográficos y/o clínicos de taponamiento.
 {jwplayer}&file=eco_ucip_video2.mp4&popup.overidetext=Vídeo 2&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video2.mp4&popup.overidetext=Vídeo 2&jwversion=5_html5{/jwplayer} 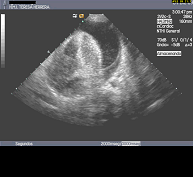 {jwplayer}&file=eco_ucip_video3.mp4&popup.overidetext=Vídeo 3&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video3.mp4&popup.overidetext=Vídeo 3&jwversion=5_html5{/jwplayer}
-Movilidad diafragmática:
La evaluación de la movilidad diafragmática es sencilla por ecografía, y tiene mucho interés en el diagnóstico, en la diferenciación entre paresia y parálisis y en el seguimiento de la evolución.
Para evaluar la función del diafragma utilizaremos sondas convexas de 3-5MHz en el eje subcostal eje corto (fig. 8). Una vez localizado el diafragma (como una línea hiperecogénica que delimita el parénquima pulmonar por su parte inferior), valoraremos, en modo B su movilidad. Observaremos que el movimiento normal de un diafragma es acercarse al transductor en inspiración y alejarse en expiración.
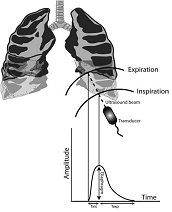 Figura 8
Figura 8
En la observación del movimiento tendremos en cuenta la amplitud del mismo además de la dirección. Una vez valorado cada diafragma por separado en modo B, se realiza un corte en Modo M de cada uno de ellos para continuar la evaluación, dónde si el movimiento es normal aparecen ondas positivas claras en el mismo.
Como se muestra en la figura 9, dónde existe una paresia diafragmática izquierda, en el modo B, vemos como el diafragma derecho se acerca transductor en inspiración (a) y se aleja en expiración (b), mientras que sucede lo contrario en el lado izquierdo que es el parético. Si realizamos un corte en modo M del diafragma derecho observaremos los picos normales durante la inspiración (c), mientras en el lado izquierdo apenas se insinúan estas líneas.
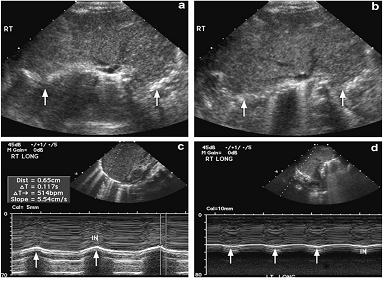 Figura 9
Figura 9
En el siguiente video (video 4) podemos ver una paresia diafragmática izquierda con su correspondencia en modo M (fig. 10).
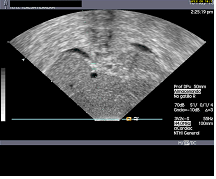 {jwplayer}&file=eco_ucip_video4.mp4&popup.overidetext=Vídeo 4&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video4.mp4&popup.overidetext=Vídeo 4&jwversion=5_html5{/jwplayer} 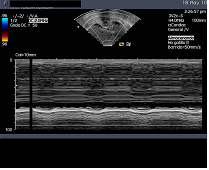 Figura 10
Figura 10
En la figura 11 podemos observar una secuencia temporal en modo M de la recuperación de la movilidad de un diafragma.
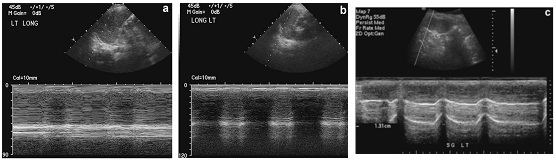 Figura 11
Figura 11
-Ecografía abdominal:
En este campo, además de la ecografía FAST en el paciente politraumatizado, que ocupará un capítulo independiente, nos vamos a centrar en la valoración y colocación de drenajes de colecciones peritoneales/ascitis, la valoración del flujo renal arterial como marcador y ajuste de drogas vasoactivas, la valoración de la vejiga (existencia de globo, colocación de sondas), y la colocación de sondas intestinales y gástricas.
-Colecciones intrabdominales:
Para la valoración abdominal precisaremos sondas convexas de bajas frecuencias, 2,5 – 5MHz, ya que lo que valoraremos serán estructuras profundas y con una superficie de exploración amplia. Aplicando el transductor sobre la pared abdominal lo reorientaremos hacia el ángulo espleno-renal, el ángulo hepato-renal y el fondo de saco de Douglas en la búsqueda de líquido libre indicativo de ascitis (fig. 12) o de la existencia de colecciones. Para identificar estas últimas hay que tener en cuenta que se modificarán menos con la presión del transductor sobre ellas y con los cambios de posición del paciente. Debemos tener especial atención a la interferencia que puede provocar el gas del interior de las asas intestinales durante la exploración.
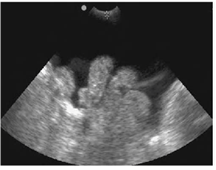 Figura 12
Figura 12
Es posible, sencillo y muy recomendable la punción de la ascitis (fig. 13) o colecciones, así como la colocación de catéteres para diálisis peritoneal, guiadas mediante ecografía para valorar los órganos próximos y evitar la punción accidental de alguno de ellos durante el procedimiento.
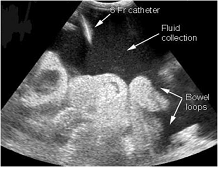 Figura 13
Figura 13
-Valoración del flujo renal:
Es relativamente sencilla la valoración por ecografía del flujo renal arterial. Mediante una sonda convexa de baja frecuencia nos colocaremos en la fosa renal y localizaremos el riñón. Tras esto realizaremos un corte trasverso del riñón y con la modalidad Doppler pulsado localizaremos el flujo pulsátil, y por tanto arterial, de los vasos renales. Debemos buscar una distribución normal del flujo en arterial renal como se muestra en las figuras 14 y 15.
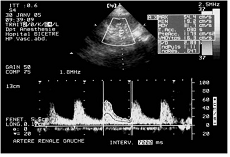 Figura 14
Figura 14 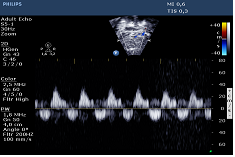 Figura 15
Figura 15
Cuando existe un exceso de drogas vasoactivas se produce una vasoconstricción importante a nivel del flujo renal, lo que produce un cambio en el patrón de flujo Doppler (fig. 16). Estos cambios también pueden verse en los fallos renales prerrenales y en la vasoconstricción de los estados de shock. Característicamente un Índice de Resistencia (IR) > 0,7 indica vasoconstricción importante.
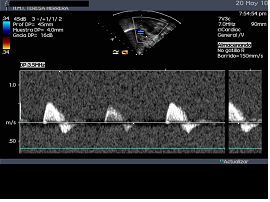 Figura 16
Figura 16
-Valoración de la Vejiga:
Es posible mediante ecografía la valoración de la vejiga. Mediante una sonda convexa colocada a nivel suprapúbico, en eje transverso y con una frecuencia adecuada según el panículo adiposo (en niños suele ser suficiente una de 5MHz). Buscaremos la vejiga, esta puede estar vacía como se muestra en la figura 17. Podemos identificar la existencia de globo vesical, veremos una formación redondeada, mientras que cuando se esta llenando adquiere una forma cuadrangular característica (fig 18).
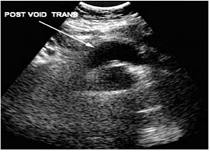 Figura 17
Figura 17 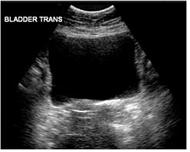 Figura 18
Figura 18
Es posible la realización de punciones suprapúbicas guiadas por ecografía. De la misma manera es posible la visualización de una sonda vesical en vejiga buscando el balón inflado en el interior de la misma (fig. 19).
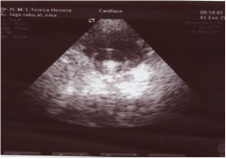 Figura 19
Figura 19
-Sondas gástricas e intestinales:
Aunque es muy compleja su adecuada visualización, es posible localizar sondas en estómago o intestino y guiar su colocación, lo que sería especialmente importante en algunos sondajes como la colocación de sondas transpilóricas sin precisar radiar al paciente. Como se ve en la figura 20, se pueden identificar sondas (N) con claridad avanzando desde el esófago (E) hasta el estómago (St) pasando bajo el hígado (L). Es una técnica compleja que precisa mucha experiencia por parte del explorador.
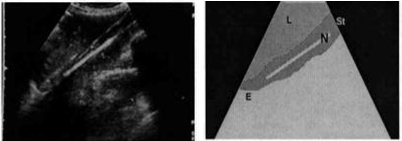 Figura 20
Figura 20
Ecografía FAST:
El acrónimo FAST se refiere a las siglas de la frase "The Focused Assessment with Sonography for Trauma", y hace referencia a las exploraciones ecográficas rápidas a realizar en un paciente politraumatizado para buscar datos de sangrado o líquido libre que puedan indicar lesión de vísceras durante el traumatismo. Esta secuencia de exploraciones ha demostrado en diversos estudios ser útil en adultos, ya que parece disminuir la necesidad de exploraciones cruentas sobre el abdomen en pacientes politraumatizados, si bien su uso es controvertido, sobre todo en pacientes pediátricos. La secuencia de exploraciones consiste en la valoración de los ángulos perihepático (fig. 21) y periesplénico, zona suprahepática y fondo de saco de Douglas, existencia de derrame pleural y pericárdico. Esencialmente lo que se busca es encontrar algún dato anormal en la exploración de estas zonas en el paciente, para posteriormente realizar otras pruebas más específicas o tomar decisiones terapéuticas urgentes en el paciente inestable. En niños tiene menos valor por que suele haber lesiones de órganos sólidos sin líquido libre y se suelen manejar de una forma más conservadora. Aunque es cierto que sirve como una primera aproximación.
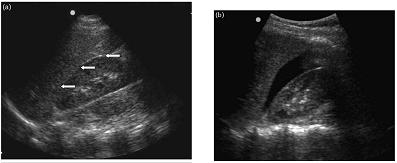 Figura 21
Figura 21
Como es el caso de la figura 21 se ve el ángulo hepato-renal normal (a) y una imagen con una colección hipoecogénica (b) que corresponde a sangre en esa misma localización.
Ecografía vascular:
El uso de la ecografía para la canalización de venas centrales y periféricas y canalización arterial tiene especial interés en la UCIP, aunque también es muy útil para la determinación de la posición de los catéteres y el diagnóstico de trombosis asociado o no a catéteres.
- Canalización de accesos vasculares.
La utilización de la ecografía para la consecución accesos vasculares en los pacientes cobra cada vez más importancia en las unidades de cuidados intensivos y en especial en la UCIP. De hecho en los estándares de calidad en la consecución de accesos vasculares centrales se considera la punción y canalización de los mismos guiados con ecografía como el Gold Estándar desde el año 2001. Es especialmente interesante en las canalizaciones dificultosas, en las de alto riesgo, en la enseñanza y para la elección de la mejor zona de acceso. En cualquier caso la punción guiada con ecografía parece ser más segura y acortar el tiempo de la técnica si se hace en cualquier circunstancia.
- Canalizaciones dificultosas: aquellas en las que existe alguna dificultad física o local como hematomas, edema, lesiones cutáneas, obesidad. También son consideradas difíciles aquellas en las que fue difícil conseguir un acceso vascular, guiado o no por ecografía, aquellos que presentaron complicaciones previas en las punciones vasculares o en los que es conocida una anatomía vascular anormal (primaria o secundaria).
- Canalización de alto riesgo: se consideran aquellas que presentaron complicaciones previas o que tiene alguna característica que favorece la aparición de complicaciones como la anticoagulación, la coagulopatía.
- Canalización en la enseñanza: diferentes estudios han mostrado mayor seguridad y eficacia en la enseñanza en la canalización de accesos vasculares si esta se realiza guiada por ecografía, e incluso se disminuye el tiempo de realización de la técnica.
- Elección de la zona de acceso: la evaluación de las posibles zonas de punción y valoración del vaso por ecografía permite elegir el vaso más óptimo para la técnica y de esta forma una consecución más rápida, segura y con menor número de tentativas. También nos permite valorar el tamaño de los catéteres de elección en función del calibre del vaso.
Es posible utilizar la ecografía para la canalización de accesos vasculares venosos centrales y periféricos, así como para la canalización y punción de vasos arteriales. Lo adecuado es la utilización de la ecografía en modo B en cortes trasversales de los vasos para la localización de éstos y longitudinales para la canalización, apoyados por el Doppler simple y color para una mejor identificación. También es posible canalización con sistema Doppler sin imagen mediante la guía con el sonido del paso de la sangre a través de los vasos (continuo en los venosos y pulsátil en los arteriales).
Los vasos que se buscan para las canalizaciones son estructuras superficiales, por lo que necesitaremos sondas de alta frecuencia (7,5-10MHz) que nos permitirán una buena definición de los mismos y preferentemente planas para una mejor identificación y delimitación del trayecto vascular.
A la hora de identificar una vaso encontraremos en corte trasversal (siempre guiados por los conocimientos anatómicos) estructuras redondeadas en las que se observa flujo con el Doppler. Para diferenciar una vena de una arteria hay que tener en cuenta:
• Arterias: aspecto redondeado, pulsátil, no colapsable con la sonda y con flujo Doppler típico especulado arterial (fig. 22).
• Venas: aspecto irregular, alargado, no pulsátil, colapsable con la sonda y que aumenta de tamaño con las maniobras de Valsava (fig. 23). El flujo Doppler es continuo.
En la figura 24 podemos identificar estas características en un corte trasversal de la arteria carótida y vena yugular derechas.
Con el Doppler color, cuando tenemos un corte con arteria y vena, veremos dos estructuras con colores diferentes de flujo (uno se aleja y el otros se acerca al transductor) (fig. 25).
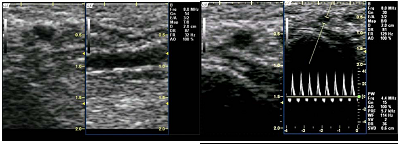 Figura 22
Figura 22
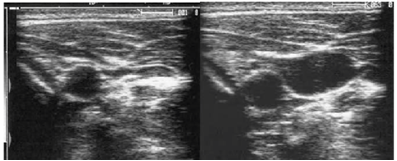 Figura 23
Figura 23
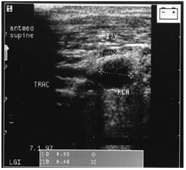 Figura 24
Figura 24 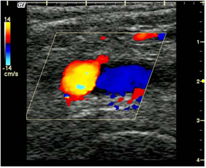 Figura 25
Figura 25
Es necesario un conocimiento anatómico de los vasos para iniciar el proceso. Ponemos el ejemplo de la distribución esquemática y en ecografía de los vasos cervicales (vena yugular derecha y arteria carótida derecha) en la figura 26 y la disposición de los vasos femorales derechos en la figura 27.
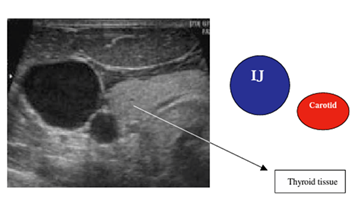 Figura 26
Figura 26
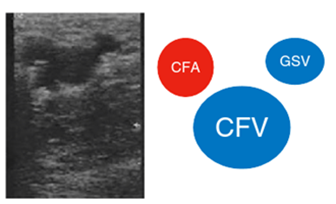 Figura 27
Figura 27
Una vez identificados los vasos en corte trasversal, girando el transductor 90º, conseguimos un corte longitudinal del vaso. En esta proyección es más sencillo guiarse para su canalización. Para la canalización de accesos vasculares guiados por ecografía existen equipos sonolucentes de técnica de Seldinger y, sobre todo agujas sonolucentes, que aunque no son imprescindibles si son muy útiles ya que son fácilmente visibles. En la figura 28 se muestra una secuencia de canalización de la vena yugular derecha con técnica de Seldinger con material convencional.
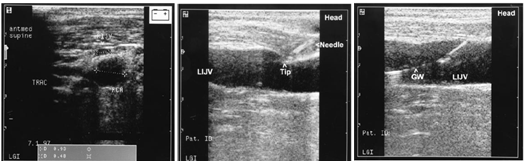 Figura 28
Figura 28
-Localización de catéteres:
Es posible mediante ecografía localizar la posición de catéteres centrales. Sobre todo es útil para valorar si se posicionan en el interior del corazón. Se muestran dos videos ejemplo dónde se visualiza un catéter en aurícula derecha (video 5) y otro en aurícula izquierda (video 6) tras atravesar el septo interauricular.
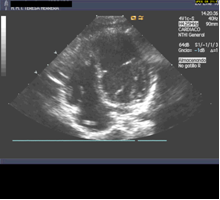 {jwplayer}&file=eco_ucip_video5.mp4&popup.overidetext=Vídeo 5&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video5.mp4&popup.overidetext=Vídeo 5&jwversion=5_html5{/jwplayer} 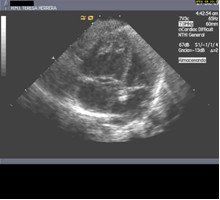 {jwplayer}&file=eco_ucip_video6.mp4&popup.overidetext=Vídeo 6&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video6.mp4&popup.overidetext=Vídeo 6&jwversion=5_html5{/jwplayer}
Si inyectamos SSF agitado previamente a través del catéter es más sencillo visualizar su posición al aparecer "burbujas" en el extremo distal del catéter (video 7).
 {jwplayer}&file=eco_ucip_video7.mp4&popup.overidetext=Vídeo 7&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video7.mp4&popup.overidetext=Vídeo 7&jwversion=5_html5{/jwplayer}
-Trombosis intravasculares:
La visualización de un material ecogénico en el interior de la luz de un vaso, asociado a un catéter o no, nos indica la presencia de un trombo en su interior.
Se muestran varias imágenes de un trombo en localización femoral (fig. 29) tanto en cortes trasversales como longitudinales asociados a un catéter. En estos casos se evidencia que al comprimir el vaso con la sonda el material queda en el interior del vaso y no permite su colapso completo.
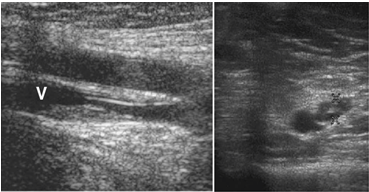 Figura 29
Figura 29
Ecografía cerebral:
Aparte de la valoración del sistema nervioso central por ecografía transfontanelar, la evaluación del flujo cerebral con ecografía –Doppler es una herramienta muy útil en la UCIP. Es una prueba cada vez más clave en el diagnóstico de la muerte encefálica, pero también es muy útil para valorar pacientes con vasoespasmo cerebral, hipertensión endocraneal, meningitis, encefalopatía hipóxico isquémica y traumatismo craneoencefálico.
Para realizar una valoración del flujo arterial cerebral necesitamos un aparato de ecografía con Doppler pulsado y una sonda de 2-2,5MHz, ya que vamos a explorar una estructura vascular profunda a través del hueso que apenas permite el paso de los ultrasonidos. Por este motivo necesitamos una sonda de alta penetrancia. Hemos de buscar zonas craneales con "buena ventana", es decir, zonas que permitan al máximo el paso de los ultrasonidos, que son zonas de menor espesor óseo. Aunque existen varias ventanas posibles (fig. 30), es la ventana transtemporal para valoración de la arteria cerebral media (ACM), ya que es la de menor profundidad y mejor acceso.
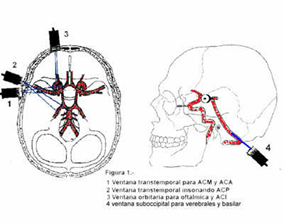 Figura 30
Figura 30
 Figura 31
Figura 31 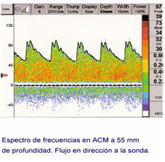 Figura 32
Figura 32
Aplicaremos el transductor en la fosa temporal y localizaremos el flujo cerebral de la ACM, realizaremos un estudio Doppler pulsado y valoraremos el patrón de flujo cerebral, la velocidad sistólica y diastólica y los índices de pulsatibilidad y resistencia. De esta forma veremos como llega la sangre arterial al cerebro, en las figuras 31 y 32 muestran un esquema y un patrón del flujo normal, respectivamente. Podemos valorar el tipo de patrón anormal función del tipo de resistencia al flujo de sangre (fig: 33):
• De alta resistencia (fig. 34): velocidades altas e índices altos, que indica flujo cerebral disminuido como en el caso de la hipertensión endocraneal, hipotensión, zonas de vasoespasmo, tumores.
• De baja resistencia (fig. 35): velocidades bajas e índices bajos, que indica flujo cerebral elevado como en hiperemia (vasodilatación cerebral) o en zonas posteriores al vasoespasmo.
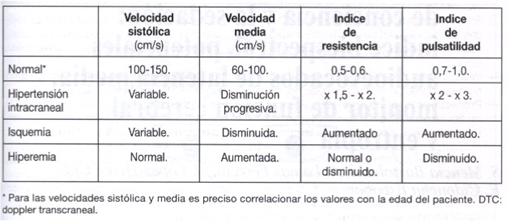
Figura 33
La valoración del flujo debe ser evolutiva para ver los cambios de patrones y la evolución del flujo. Esto nos dará idea de la evolución de la lesión.
 Figura 34
Figura 34 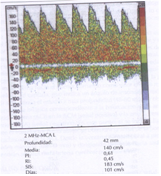 Figura 35
Figura 35
En el caso de la muerte cerebral se evidenciará un patrón inicial de aumento de resistencia del flujo con reducción del flujo sistólico e inversión del diastólico de tipo reverberante (fig. 36), que es ominoso y precede al cese del flujo cerebral, posteriormente aparecen espigas sistólicas (fig. 36) que indican ausencia de flujo cerebral y por lo tanto muerte cerebral. En estadio muy avanzado existe ausencia de señal.
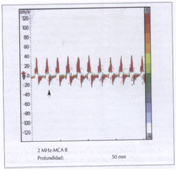 Figura 36
Figura 36 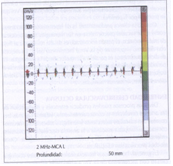 Figura 37
Figura 37
El uso del flujo Doppler cerebral es relativamente sencillo, reproducible y nos permite una valoración evolutiva de los pacientes, si bien es necesario un adiestramiento, es poco específico y, en ocasiones, no existe una buena ventana para la valoración.
Otros usos de la ecografía en UCIP:
La ecografía es una herramienta muy versátil y cada vez con mayor utilización. Permite la exploración de muchas zonas del organismo de una forma sencilla y rápida, y sin repercusión para el paciente. Por este motivo puede ser utilizada para la valoración de la vía aérea (fig. 37), posición o tamaño de tubos endotraqueales, la localización de abscesos (fig. 38) y cuerpos extraños (fig. 39 y video 8), la valoración de fracturas (fig. 40), la realización de punciones lumbares, bloqueos nerviosos, punciones articulares, biopsias guiadas por ecografía, etc.
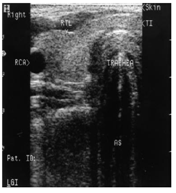 Figura 38
Figura 38 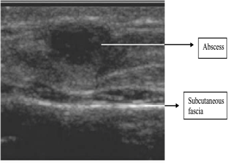 Figura 39
Figura 39
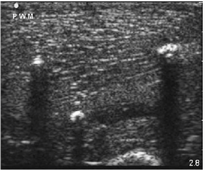 Figura 40
Figura 40 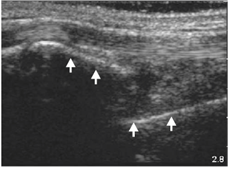 Figura 40
Figura 40
 {jwplayer}&file=eco_ucip_video8.mp4&popup.overidetext=Vídeo 8&jwversion=5_html5{/jwplayer}
{jwplayer}&file=eco_ucip_video8.mp4&popup.overidetext=Vídeo 8&jwversion=5_html5{/jwplayer}
Conclusiones:
La disponibilidad actual de aparatos de ecografía en las unidades de cuidados intensivos, sencillos de manejar y portátiles, permiten realizar diagnósticos a pie de cama del paciente, una toma de decisiones rápida y la realización de procedimientos eficientemente. Todo ello de una forma más segura para el paciente y a bajo coste. Pero es esencial el entrenamiento de los profesionales en esta técnica para evitar los errores diagnósticos, y de tratamiento, y la realización de técnicas de una forma subóptima.
Bibliografía
1. Schmidt GA. ICU Ultrasound. The coming boom. Chest. 2009 Jun;135(6):1407-8.
2. Lynch RE.Ultrasound is coming to a pediatric intensive care unit near you. Crit Care Med 2009 Mar;37(3):1170-2.
3. Mayo PH, Beaulieu Y, Doelken P et al. American College of Chest Physicians/La Société de Réanimation de Langue Française statement on competence in critical care ultrasonography. Chest 2009 Apr;135(4):1050-60.
4. Neri L, Storti E, Lichtenstein D. Toward an ultrasound curriculum for critical care medicine. Crit Care Med 2007 May;35(5 Suppl):S290-304.
5. Beaulieu Y, Marik PE. Bedside ultrasonography in the ICU: part 2. Chest 2005 Sep;128(3):1766-81.
6. Beaulieu Y, Marik PE. Bedside ultrasonography in the ICU: part 1. Chest 2005 Aug;128(2):881-95.
7. Guillory RK, Gunter OL. Ultrasound in the surgical intensive care unit. Curr Opin Crit Care 2008 Aug;14(4):415-22.
8. Levy JA, Bachur RG. Bedside ultrasound in the pediatric emergency department. Curr Opin Pediatr.2008 Jun;20(3):235-42.
9. Epelman M, Navarro OM, Daneman A, Miller SF. M-mode sonography of diaphragmatic motion: description of technique and experience in 278 pediatric patients. Pediatr Radiol. 2005 Jul;35(7):661-7. Epub 2005 Mar 18.
10. Hatfield A, Bodenham A. Ultrasound: an emerging role in the anaesthesia and intensive care. Br J Anaesth 1999; 83: 789-800.
11. Riccabona M, Sorantin E, Ring E.Application of M-mode sonography to functional evaluation in pediatric patients. Eur Radiol 1998;8(8):1457-61.
12. Bouhemad B, Zhang M, Lu Q, Rouby JJ. Clinical review: Bedside lung ultrasound in critical care practice. Crit Care 2007;11(1):205.
13. Colmenero M, García-Delgado M, Navarrete I, López-Milena G. Utility of the lung ultrasound in the intensive medicine unit. Med Intensiva 2010 Dec;34(9):620-8. Epub 2010 May 18.
14. Froehlich CD, Rigby MR, Rosenberg ES et al. Ultrasound-guided central venous catheter placement decreases complications and decreases placement attempts compared with the landmark technique in patients in a pediatric intensive care unit. Crit Care Med 2009 Mar;37(3):1090-6.
15. Shiloh AL, Eisen LA. Ultrasound-guided arterial catheterization: a narrative review. Intensive Care Med 2010; 36:214–221.
16. Kory PD, Pellecchia CM, Shiloh AL, Mayo PH, Koenig S. Accuracy of Ultrasonography Performed by Critical Care Physicians for the Diagnosis of Deep Venous Thrombosis. Chest 2010 Oct 28.
17. Rasulo FA, De Peri E, Lavinio A. Transcranial Doppler ultrasonography in intensive care. Eur J Anaesthesiol Suppl 2008;42:167-73.
18. Davison D, Junker C. Advances in critical care for the nephrologist: hemodynamic monitoring and volume management. Clin J Am Soc Nephrol 2008 Mar;3(2):554-61.
19. Hernández-Socorro CR, Marin J, Ruiz-Santana S, Santana L, Manzano JL. Bedside sonographic-guided versus blind nasoenteric feeding tube placement in critically ill patients. Crit Care Med 1996 Oct;24(10):1690-4.







